Gen aus – Fett weg?#
von
Juliane Bogner-Strauß
Institut für Genomik und Bioinformatik

Juliane Bogner-Strauß ist Associate Professorin am Institut für Genomik und Bioinformatik an der TU Graz. Gemeinsam mit ihrer Arbeitsgruppe erforscht sie die Charakterisierung von Genen, die im Fettstoffwechsel eine Rolle spielen. Zurzeit leitet sie Subprojekte im Rahmen des österreichischen Genomforschungsprogramms "GEN-AU Genomforschung in Österreich" und beim DK-plus: "Metabolic & Cardiovascular Disease".
© Forschungsjournal 2010/03
Die Fettleibigkeit ist in den letzten Jahrzehnten weltweit rasant angestiegen und stellt inzwischen nicht nur ein gesundheitliches Risiko, sondern auch ein wirtschaftliches Problem dar. Wir sind daran interessiert, Gene zu identifi zieren und zu charakterisieren, die im Fettstoffwechsel eine wichtige Rolle spielen. Dafür verwenden wir in erster Linie Zellkulturmodelle, in denen wir diese Gene nach Bedarf ein- und ausschalten können und die uns sehr schnell Antwort auf die Frage, ob diese Gene eine Rolle bei der Einlagerung von Fetten in Zellen spielen, geben. Das Interesse der pharmazeutischen Industrie, solche Gene im Rahmen therapeutischer Anwendungen zu beeinflussen, ist stark im Steigen.
Die Fettleibigkeit (Adipositas) hat in den letzten Jahrzehnten enorme Ausmaße angenommen und ist damit nicht nur ein gesundheitliches Risiko,sondern auch ein beträchtliches wirtschaftliches Problem geworden. Heute leiden weltweit gleich viele Menschen an Unterernährung wie an Adipositas (nämlich etwa je eine Milliarde). Fettleibigkeit führt zu vielen Folgeerkrankungen wie Type 2 Diabetes, erhöhte Blutfettwerte, Bluthochdruck, Atherosklerose, Herzinfarkt, Schlaganfall, Krebs, Infertilität, Arthritis und viele mehr. In Österreich sind bereits an die 50 Prozent der Bevölkerung übergewichtig und 15 Prozent von Fettleibigkeit betroffen. Als Übergewicht bezeichnet man einen Body Mass Index (BMI) von > 25, als Fettleibigkeit einen BMI von über 30. Der BMI wird wie folgt berechnet:
Gewicht in kg
Der prozentuelle Anteil an fettleibigen Personen in Österreich hat in den letzten Jahren stark zugenommen: Waren es vor 20 Jahren noch acht Prozent, so sind es heute beinahe doppelt so viele. Auch unter den sechs bis 14-jährigenÖsterreicherinnen und Österreichern leiden bereits elf Prozent an Fettleibigkeit.
Österreich liegt damit in Europa im Mittelfeld und wird global gesehen vor allem von Ländern wie den USA, Alaskaund dem Iran bei Weitem übertroffen. In diesen Ländern sind bereits über 30 Prozent der Bevölkerung von Adipositas betroffen. Weltweit sterben pro Jahr etwa 15 Millionen Menschen an Herz-Kreislauf-Erkrankungen, wie Herzinfarkt und Gehirnschlag, die aufgrund oder als Folge von Fettleibigkeit auftreten. Bei der Entstehung der Fettleibigkeit spielt die (falsche) Ernährung sicherlich die Hauptrolle. Das Problem ist "einfach": Der Körper nimmt mehr Energie zu sich, als er verbrennen kann.
Somit wird sofort ein Fettdepot angelegt – aus gutem Grund: Unser Körper ist seit Anbeginn der Menschheit nämlich darauf programmiert vorzusorgen, und zwar für "schlechte Zeiten", in denen das Essen Mangelware sein könnte. Aber auch unsere bewegungsarmen Lebensgewohnheiten spielen bei der Entstehung von Fettleibigkeit eine überaus "gewichtige" Rolle.
Natürlich gibt es auch genetische Veranlagungen für die Entwicklung der Fettleibigkeit, dazu zählen sowohl monogenetische als auch polygenetische Prädispositionen (Ausbildung eines Merkmals wie Fettleibigkeit durch ein einziges oder durch mehrere Gene). Diese sind aber wesentlich weniger relevant als der Überkonsum von Lebensmitteln und der bewegungsarme Lebensstil. Der Fettleibigkeit und den oben erwähnten Erkrankungen, die damit in Zusammenhang stehen, liegen unter anderem Fettstoffwechselstörungen zugrunde, die zur massiven Einlagerung von Lipiden (Fetten) ins Fettgewebe und in andere Gewebe wie Herzmuskel, Skelettmuskel und Leber führen.
Meine Arbeitsgruppe hat sich nun der Herausforderung verschrieben, Gene zu identifi zieren, die in der Fettzellentwicklung (Adipogenese) eine Rolle spielen, und diese Gene funktionell zu beschreiben. Man kennt heute zwar das gesamte menschliche Genom, aber nur 50 Prozent der Gene sind in ihrer Funktion aufgeklärt. Zur Auffindung von funktionell uncharakterisierten Genen,die im Fettstoffwechsel bzw. bei der Entstehung von Fettzellen eine Rolle spielen könnten, nutzen wir als ersten Schritt die Transkriptomanalyse.
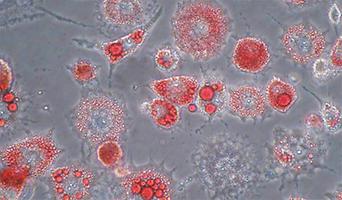
Mithilfe dieser Technik werden Vorläuferfettzellen (Präadipozyten) und Fettzellen (Adipozyten), die in Kultur gezüchtet werden, auf genetischer Ebeneverglichen. Präadipozyten und Adipozyten besitzen zwar die gleichen Gene, damit aber aus einer Vorläuferfettzelle eine Fettzelle wird, müssen bestimmte Gene hoch-, andere hinunterreguliert werden. Diese regulierten Gene können mithilfe der Transkriptomanalyse untersucht werden.
Bei diesen Experimenten sind wir in der Lage etwa 15.000 Gene zugleich auf ihre Regulation hin zu untersuchen. An diesem Punkt angelangt, kommt nun die Bioinformatik ins Spiel. Eine Auswertung eines solchen Experiments von Hand würde wohl Monate in Anspruch nehmen, mithilfe der Bioinformatik gelingt das, je nach Umfang des Experiments, innerhalb weniger Stunden bzw. Tage. Das Ergebnis ist eine Liste von funktionell charakterisierten und – für uns noch interessanter – funktionell nicht charakterisierten Genen, die bei der Entstehung der Fettzelle reguliert sind. In einem nächsten Schritt werden diese Gene einzeln in Zellen in Kultur überproduziert oder ausgeschaltet. Die Konsequenzen können nun weitreichend sein, zum Beispiel kann dieÜberproduktion oder eben das Ausschalten eines Gens in Vorläuferfettzellen dazu führen, dass aus diesen Präadipozyten keine Fettzellen mehr werden. Natürlich ist auch das umgekehrte Szenario möglich, d. h., das Ausschalten oder die Überproduktion eines Gens führt dazu, dass Präadipozyten noch effizienter Fett einlagern.
Zurzeit arbeiten wir an einem Gen, dessen Produktion notwendig ist, um aus Vorläuferfettzellen Fettzellen zu machen. Schalten wir das Gen in Zellen in Kultur aus, sind diese nicht mehr in der Lage, Lipide einzulagern. Der nächste Arbeitsschritt in unserem Labor ist, dieses Gen in Mäusen auszuschalten, um zu erforschen, ob diese Mäuse auch nicht mehr in der Lage sind, Fettgewebe aufzubauen.
Die Identifizierung solcher Gene und deren funktionelle Charakterisierung haben natürlich immense
Auswirkungen auf das Verständnis der Regulation des Fettstoffwechsels. Dementsprechend groß ist in Zeiten der zunehmenden Fettleibigkeit und den damit in Zusammenhang stehenden Erkrankungen das Interesse der pharmazeutischen Industrie, solche Gene als Ziele in der therapeutischen Anwendung zu beeinflussen.