Molekulare Bildgebung#
mittels Magnetresonanz-Imaging und Fluoroptischer Tomografie#
von
Rudolf Stollberger, Hermann Scharfetter
Institut für Medizintechnik


Rudolf Stollberger ist Leiter des Instituts für Medizintechnik. Seine Forschungsinteressen liegen im Bereich der Entwicklung und Verbesserung medizinischer Bildgebungsverfahren für die Gewinnung von funktioneller, molekularer und biophysikalischer Information, insbesondere mithilfe der Magnetresonanz.
© Forschungsjournal 2010/03
Am Institut für Medizintechnik wird an neuen Bildgebungstechniken gearbeitet, die es erlauben, biologische Prozesse auf zellulärer und molekularer Ebene in vivo sichtbar zu machen, zu charakterisieren und zu quantifizieren. Dieses junge Feld der biomedizinischen Bildgebung, auch "Molekulares Imaging" genannt, wird als wesentliches Zukunftsfeld für die Entwicklung einer individualisierten oder zumindest stratifi zierten Medizin gesehen. Die Herausforderungen ergeben sich aus der Inter- und Multidisziplinarität, die durch die Überschneidung medizinischer Fragestellungen und Anwendungen mit der Erforschung der zugrunde liegenden biologischen Prozesse, der Entwicklung von molekularen Sensoren und von neuen Bildgebungstechnologienund Auswerteverfahren bedingt ist.
Molekulares Imaging beruht in den meisten Fällen auf der Verwendung von Zielfindungsmolekülen, die spezifi sch an einen molekularen Markerim Gewebe ankoppeln oder an einem biologischen Prozess teilnehmen.
Diese Moleküle sind inhärent mit einer Komponente verknüpft, die mit bildgebenden Verfahren detektiert werden kann. Solche selektiv bindenden Strukturen können z. B. pegylierte Liposomen (PEG-Liposoms) sein, die mit Targeting-Molekülen wie z. B. globular Adiponektin selektiv an endothelialen Zellen in entzündeten Bereichen anhaften und diese markieren.
Der In-vivo-Nachweis der gebundenen Partikel mithilfe der MR-Tomografie (MRT) kann nun z. B. über in die Liposomen eingebrachte paramagnetische Eisenoxyde erfolgen. Wie sich diese Moleküle an unterschiedlichen Stellen im Körper auf die MR-Bildgebung auswirken, ist von einer Vielzahl von Faktoren, den verwendeten Untersuchungssequenzen und der Gerätekonfiguration abhängig. Um sowohl die Bildgebung als auch die verwendeten Sensormoleküle zu optimieren, ist es essenziell, die physikalischen Grundlagen der NMR-Signalentstehung für diese Anwendungen genau zu verstehen und zu untersuchen.
Dies und das Erreichen einer möglichst quantitativen Darstellung der räumlich-zeitlichen Verteilung der Nanopartikel ist Ziel der Forschungstätigkeit am Institut für Medizintechnik. Im Rahmen des Verbundprojekts Nano-Health der FFG werden zurzeit zwei Anwendungen der molekularen/zellulären Bildgebung bearbeitet. Die Kooperationspartner in diesem Projekt sind Ruth Prassel von der Österreichischen Akademie der Wissenschaften, Harald Mangge und Dirk Strunk von der Medizinischen Universität Graz und Andreas Zimmer von der Karl-Franzens-Universität Graz.
Gefäßwand
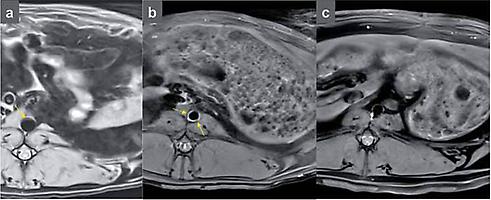
(a) Erste strukturelle Änderungen in der Aorta eines Watanabe-Hasen (Protonendichte gewichtet TSE-Sequenz)
(b) Darstellung von entzündlichen Prozessen in einer Gefäßwand ohne dedizierte Plaques durch selektive Anlagerung von Gadofluorin (24 h post Gadofl uorin, T1-gewichtet TSE Sequenz)
(c) Kontrolluntersuchung mit Gadofluorin mit einem gesunden New-Zealand-Hasen (24 h post Gadofl uorin, T1-gewichtet TSE Sequenz)
© Forschungsjournal 2010/03 / Institut für Medizintechnik
Die Charakterisierung der Morphologie arteriosklerotischer Veränderungen und die daraus resultierenden Gefäßverengungen ist eine wichtige Aufgabe für die vaskuläre Bildgebung und beschreibt den vorläufigen Endzustand einer Arteriosklerose.
Für ein tieferes Verständnis des Krankheitsstatus und für das Monitoring des Verlaufes ist es von eminenter Bedeutung, Informationen über zugrunde liegende Prozesse und Parameter zu bekommen, zu denen u. a. der Entzündungsstatus der Gefäßwand gehört. Mittels fluoroptisch markierter Nanopartikel an operierten Aorten von ApoEdefizienten Mäusen konnten Entzündungsparameter bereits erfolgreich nachgewiesen werden. Gegenwärtig wird die Anwendbarkeit von MR-Bildgebung für den In-vivo-Nachweis von Entzündungsparametern in einem Watanabe-Hasenmodell untersucht (Abb. 1).
In weiterer Folge soll durch spezifisch entwickelte HF-Empfangsspulen die Erkennbarkeit (Kontrast- Rausch-Verhältnis) weiter verbessert werden und eine Quantifizierung der Bindung der Nanopartikel mittels neuer biophysikalischer Modelle erfolgen. Herausforderungen für die Medizintechnik ergeben sich also sowohl in der Scanmethodik als auch in der Hardware und der Signalanalyse mittels geeigneter mathematischer Methoden.
Stem Cell
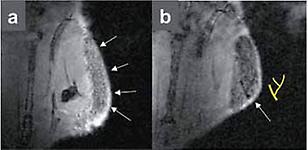
(a) Verteilung der Zellen nach Injektion (Pfeile)
(b) Entwicklung von Gefäßstrukturen nach zwei Wochen (siehe auch Zeichnung daneben)
© Forschungsjournal 2010/03 / Institut für Medizintechnik
Eine andere höchst spannende Anwendung ist die Verfolgung von transplantierten Stammzellen. Es wird generell angenommen, dass Stammzellen in bestimmte Gewebe wandern und sich dort in vorhersehbarer und erwünschter Weise weiterentwickeln. Diese Annahmenmüssen aber für verschiedene therapeutische Ansätze in vivo überprüft und validiert werden. Eine besondere Herausforderung besteht darin, dass die sensitivste Markierung der Stammzelle mittels superparamagnetischer Eisenoxyde bislang zu negativem Kontrast der Zellen führt. Im Rahmen unserer Arbeiten konnte nun gezeigt werden, dass mittels einer "Ultra Short Echo Time"-Sequenz (UTE) bei primär positivem Kontrast höchst aufgelöste Bilder von markierten Stammzellen erzielt werden können. In anderen In-vivo-Untersuchungen konnte mit konventioneller Scantechnik gezeigt werden, dass endotheliale Vorläuferzellen tatsächlich Gefäße bilden (Abb. 2).
Weitere Entwicklungsrichtungen (Integrated Dual Modality Imaging)
Ein essenzielles Grundproblem der molekularen Bildgebung besteht darin, dass die verfügbaren Modalitäten typischerweise nur entweder eine hohe Sensitivität für Sensormoleküle oder eine gute morphologische Darstellung ermöglichen. Dies hat in der Humanmedizin zur Entwicklung hybrider Systeme, wie PET-CT, und zur Forschung im Bereich PET-MR geführt. In der präklinischen Forschung wird mit Kleintiermodellen gearbeitet. Diese ermöglichen auch die Verwendung einer Vielzahl etablierter fluoroptischer Marker.
© Forschungsjournal 2010/03 / Institut für Medizintechnik
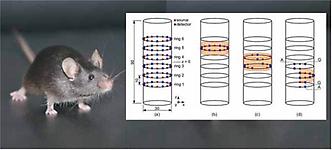
Um die Defizite des konventionellen (2-D) In-vivo-Fluoreszenzimagings zu überwinden, wird an fluoroptischen Tomografieverfahren (FDOT) gearbeitet. Diese Verfahren können noch wesentlich verbessert werden, wenn morphologische Information zur Rekonstruktion der Fluoreszenzbilder herangezogen wird, was hervorragend durch die Kombination von FDOT und MRT erreicht werden kann. An einer solchen Kombination wird intensiv in der Arbeitsgruppe "Near Field Imaging" gearbeitet. Diese Modalität kombiniert moderne Lasertechnologie, hochsensitive optische Detektoren und MR-Spulenbau mit der Entwicklung komplexer mathematischer Algorithmen aus dem Bereich der inversen Probleme sowie aufwendigen Registrierungs- und Bildverarbeitungsmethoden (Abb. 3).
Die Arbeitsgruppe hat bereits im Rahmen des SFB "Mathematical Optimization and Applications in Biomedical Sciences" ein Verfahren zur Optimierung der Sensor-Detek tor- Positionen hinsichtlich des Signal- Rausch-Verhältnisses sowie Verbesserungen bisheriger fluor optischer 3-D-Bildrekonstruktionsalgorithmen entwickelt und treibt nun die Entwicklung eines Systems voran, das die Rekonstruktion biochemischer Information aus der Fluoreszenzlebensdauer ermöglichen soll.