Adenin
| Strukturformel | |||||||||
|---|---|---|---|---|---|---|---|---|---|
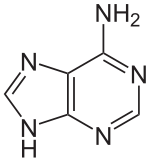 |
|||||||||
| Allgemeines | |||||||||
| Name | Adenin | ||||||||
| Andere Namen |
|
||||||||
| Summenformel | C5H5N5 | ||||||||
| Kurzbeschreibung | hellgelber Feststoff[1] |
||||||||
| Externe Identifikatoren/Datenbanken[Ein-/ausblenden] | |||||||||
| CAS-Nummer | 73-24-5 | ||||||||
| PubChem | 190 | ||||||||
| DrugBank | DB00173 | ||||||||
| Wikidata | Q15277 | ||||||||
| Arzneistoffangaben | |||||||||
| ATC-Code | |||||||||
| Eigenschaften | |||||||||
| Molare Masse | 135,13 g·mol−1 | ||||||||
| Aggregatzustand | fest |
||||||||
| Schmelzpunkt | Sublimation bei 220 °C[2] |
||||||||
| Siedepunkt | Zersetzung ab 360 °C[2] |
||||||||
| Löslichkeit | schlecht in Wasser[2] |
||||||||
| Sicherheitshinweise | |||||||||
|
|||||||||
| Toxikologische Daten | |||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||
Adenin (A, Ade) ist eine der vier wichtigsten Nukleinbasen in der DNA und RNA, zusammen mit Cytosin, Guanin und Thymin (Uracil in RNA). Es ist eine heterocyclische organische Verbindung mit einem Puringrundgerüst und einer Aminogruppe in 6-Stellung. Die Nukleoside von Adenin sind das Desoxyadenosin in der DNA und das Adenosin in der RNA. In der Watson-Crick-Basenpaarung bildet es zwei Wasserstoffbrücken mit Thymin bzw. Uracil.
Darstellung
- Lord-Todd-Synthese angewandt auf Formamidin und Phenylazomalononitril.
- Adenin kann als Pentamer der Blausäure angesehen werden und in flüssigem Ammoniak mit Ausbeuten von über 20 % aus dieser dargestellt werden.[4]
Biologische Bedeutung
Adenin kann Bestandteil der DNA, RNA oder verschiedener Nukleoside und Nukleotide sein.
Nukleoside
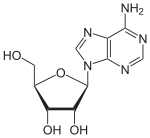
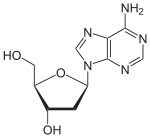
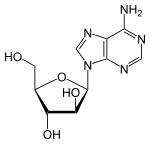
Über das N9-Atom des Fünfringes kann Adenin an das C1-Atom der Ribose N-glycosidisch gebunden werden; man spricht dann von einem Nukleosid, dem Adenosin. Bei der Bindung an Desoxyribose entsteht das Nukleosid Desoxyadenosin. Das synthetische Vidarabin enthält – im Gegensatz zu den meisten Nukleosiden – anstelle der Ribose die Arabinose.
Nukleotide
An Adenosin kann Phosphorsäure als Phosphatrest gebunden sein, so entstehen
- Adenosinmonophosphat (AMP)
- Cyclisches Adenosinmonophosphat (cAMP)
- Adenosindiphosphat (ADP)
- Adenosintriphosphat (ATP)
Entsprechende Moleküle entstehen, wenn die Phosphatreste an Desoxyadenosin gebunden werden (dAMP; dADP; dATP).
Adenosintriphosphat (ATP) spielt eine besondere Rolle im Energiestoffwechsel der Zelle. Durch die Reaktion ATP → ADP + P wird Energie frei, durch die Reaktion ADP + P → ATP wird Energie chemisch gespeichert.
Cyclisches Adenosinmonophosphat (cAMP) ist ein sehr verbreiteter Second Messenger der zellulären Signaltransduktion.
Adenin ist außerdem Bestandteil des Nicotinamidadenindinucleotids NAD+, das als Coenzym der Wasserstoffübertragung dient und so in der Zelle bei Redox-Reaktionen beteiligt ist. Adenin wird zur Biosynthese des Coenzyms S-Adenosyl-Methionin verwendet, welches bei biologischen Methylierungen Einsatz findet.
Bestandteil der DNA und RNA
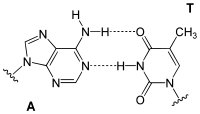
Adenin bildet in der DNA-Doppelhelix zwei Wasserstoffbrücken mit Thymidin aus. Bei der Transkription dagegen paart sich das Adenin des codogenen Strangs der DNA mit dem Uridin der gerade gebildeten mRNA. In der tRNA gibt es zudem Paarungen mit Dihydrouridin oder Pseudouridin.
 |
 |
 |
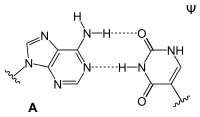 |
| A-T-Basenpaar (DNA) | A-U-Basenpaar (RNA) | A-D-Basenpaar (RNA) | A-Ψ-Basenpaar (RNA) |
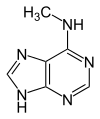
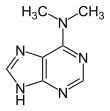
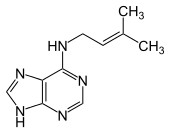
Verwandte Verbindungen
 |
 |
 |
 |
 |
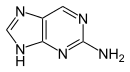 |
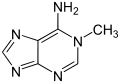
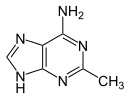
| 1-Methyladenin | 2-Methyladenin | N6-Methyladenin | N6,N6-Dimethyladenin | N6-Isopentenyladenin | 2-Aminopurin (Isoadenin) |
Einzelnachweise
- ↑ Datenblatt Adenin (PDF) bei Carl Roth, abgerufen am 14. Dezember 2010.
- 1 2 3 Thieme Chemistry (Hrsg.): RÖMPP Online - Version 3.5. Georg Thieme Verlag KG, Stuttgart 2009.
- 1 2 3 Datenblatt Adenine bei Sigma-Aldrich, abgerufen am 20. März 2011 (PDF).
- ↑ Albert Gossauer, Struktur und Reaktivitat der Biomoleküle: Eine Einführung in die organische Chemie, Verlag Helvetica Chimica Acta, 2006.
Weblinks
- Eintrag zu Adenine in der Human Metabolome Database (HMDB), abgerufen am 19. November 2013.
- Vorlage:Wikigenes