Schalenmodell (Atomphysik)
Das Schalenmodell ist ein Atommodell, bei dem die Elektronen den Atomkern in konzentrischen Schalen umgeben. Der Aufenthaltsort eines Elektrons wird durch eine Wahrscheinlichkeitsfunktion modelliert. Die Amplitude dieser Funktion an einem bestimmten Ort ist proportional zur Aufenthaltswahrscheinlichkeit des Elektrons an diesem Ort. Das Schalenmodell ist damit eine Vereinfachung des Orbitalmodells.
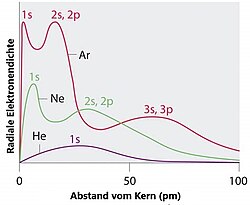
Nach diesem Modell sind die Elektronen in der Atomhülle in Schalen angeordnet, anschaulich etwa wie die Schalen einer Zwiebel. Jede Schale ist der räumliche Aufenthaltsbereich von Elektronen mit ähnlichen Bindungsenergien. Die innerste, dem Atomkern nächstgelegene Schale wird K-Schale genannt. Sie enthält maximal zwei Elektronen. Auf der nächsten Schale, der L-Schale finden maximal acht Elektronen Platz. Generell fasst die n-te Schale 2·n2 Elektronen.
Die Schalen sind nochmals untergliedert in „Unterschalen“ mit 2, 6, 10 … Elektronen. Für die chemischen Eigenschaften der Hauptgruppenelemente ist vor allem die Zahl der Elektronen in den ersten beiden Unterschalen der äußersten Schalen entscheidend.
Die Anzahl der Schalen eines Elementes entspricht im Periodensystem der Elemente der Nummer der Periode: Elemente der 1. Periode haben eine Schale, die der 2. Periode zwei Schalen, die der 3. Periode drei Schalen usw.
Eigenschaften der Elemente
Mit dem Schalenmodell der Atome lassen sich verschiedene Eigenschaften der Elemente gut erklären, da jedes Atom seine Edelgaskonfiguration, acht Elektronen in der Außenschale, „anstrebt“. Beispiele:
- Alkalimetalle besitzen nur ein einziges Außenelektron (Valenzelektron) und können dieses daher besonders leicht abgeben; d. h., ihre Ionisierungsenergie ist gering. Daher sind Alkalimetalle besonders reaktiv.
- Den Halogenen fehlt nur ein Elektron für eine voll besetzte Außenschale, daher nehmen sie leicht Elektronen von anderen Elementen auf (z. B. von Natrium) und sind dadurch ebenfalls sehr reaktiv.
- Die Edelgase besitzen bereits eine voll besetzte Außenschale und zeigen daher überhaupt keine „Neigung“, chemische Reaktionen einzugehen.
Bezeichnung und maximale Elektronenanzahl der Elektronenschalen
1911 führte Charles Glover Barkla die Bezeichnungen K und L für die beiden Komponenten der charakteristischen Röntgenstrahlung an, die man damals nur anhand ihres Durchdringungsvermögens unterscheiden konnte. Die ersten Buchstaben A, B etc. des Alphabets waren schon lange für die Absorptionslinien des Sonnenlichts in Gebrauch, und Barkla wollte die Liste für die Röntgenstrahlung gegebenenfalls nach beiden Seiten verlängern können.[2] 1913 führte Niels Bohr mit seinem Atommodell diskrete Energiezustände der Elektronen im Atom ein und nummerierte sie mit der Hauptquantenzahl . Nachdem über die Wellenlänge der Röntgenquanten ihre Energie gemessen werden konnte, stellt Walther Kossel 1914 fest, dass die K-Strahlung von dem Übergang eines Elektrons in den Zustand mit herrührte.[3] Nachdem ebenso die L-Strahlung zu passte, erhielten die Bohrschen Energieniveaus neben der Hauptquantenzahl die Namen K-, L-, ... Niveau. 1916 schloss Kossel aus dem gleichmäßigen Anwachsen der Röntgenenergien mit steigender Ordnungszahl, dass die Atome aller Elemente in ihrem inneren Aufbau ähnlich seien, während die ausgeprägten periodischen Unterschiede in ihrem chemischen Verhalten von ihren äußersten Elektronen bestimmt sind.[4] Für die Bohrschen Niveaus prägte er den Begriff Schale und nahm an, dass die Schalen mit steigender Ordnungszahl von unten her aufgefüllt werden, wobei jede Schale nur eine bestimmte Anzahl Elektronen aufnehmen könne, die bei den Edelgasen gerade erreicht sei. Ebenfalls 1916 erweiterte Arnold Sommerfeld das (ebene) Bohrsche Modell zum (räumlichen) Bohr-Sommerfeldschen Atommodell und fand zwei weitere Quantenzahlen, mit denen die quantenmechanischen Zustände, die zu derselben Hauptquantenzahl gehören, einzeln bezeichnet und ihre Gesamtzahl zu ermittelt werden konnten. Dass die Maximalzahl der Elektronen mit genau doppelt so groß ist, konnte an den Ordnungszahlen der beiden ersten Edelgase (He, Ne) abgelesen werden. Dass eine solche Maximalzahl überhaupt existiert, wurde 1923 von Wolfgang Pauli durch das Paulische Ausschließungsprinzip erklärt. Dass jeder der im Bohr-Sommerfeld-Modell mit drei Quantenzahlen benannte Zustand mit je zwei Elektronen besetzt werden kann, wurde 1925 durch S. Goudsmit und G.E. Uhlenbeck[5] mittels der zusätzlichen Spin-Quantenzahl erklärt.
Schwächen des Atom-Schalenmodells
Es gibt Phänomene, die das atomare Schalenmodell nicht erklären kann. Da es in seiner einfachsten Form den Elektronen räumlich getrennte Kugelschalen zuweist, deren Radius mit der Hauptquantenzahl anwächst, kann es den Elektroneneinfang in den Kern (eine Form der radioaktiven Umwandlung) nicht behandeln, der die Anwesenheit von Elektronen am Ort des Kerns beweist. Des Weiteren bleibt die räumliche Gestalt der Moleküle unerklärt. Warum hat z. B. das Methan (CH4) eine tetraederförmige Gestalt, oder warum ist das Wassermolekül gewinkelt? Diese Eigenschaften der Atome und Moleküle lassen sich mit dem quantenmechanischen Orbitalmodell und seinen Weiterentwicklungen wie VSEPR-Modell sowie über Hybridorbitale und Molekülorbitale erklären.
Siehe auch
Literatur
- W. Finkelnburg: Einführung in die Atomphysik. Springer Verlag, Berlin Heidelberg 1976.
Weblinks
- Atombau – Das Schalenmodell, Erklärung auf Mittelstufenniveau
Einzelnachweise
- ↑ LibreTexts: radial density distribution. LibreTexts, abgerufen am 31. Oktober 2020.
- ↑ Charles G. Barkla: XXXIX. The spectra of the fluorescent Röntgen radiations. In: The London, Edinburgh, and Dublin Philosophical Magazine and Journal of Science. Band 22, Nr. 129, September 1911, ISSN 1941-5982, S. 396–412, doi:10.1080/14786440908637137 (tandfonline.com [abgerufen am 10. Dezember 2023]).
- ↑ Walter Kossel: Bemerkung zur Absorption homogener Röntgenstrahlen. Verhandlungen der deutschen physikalischen Gesellschaft, 16 (1914), 898–909.
- ↑ Walther Kossel: Über Molekülbildung als Frage des Atombaus. Annalen der Physik Bd. 49, 1916, S. 229–362, doi:10.1002/andp.19163540302.
- ↑ G. E. Uhlenbeck, S. Goudsmit: Ersetzung der Hypothese vom unmechanischen Zwang durch eine Forderung bezüglich des inneren Verhaltens jedes einzelnen Elektrons. In: Naturwissenschaften. Band 13, Nr. 47, 1925, S. 953–954, doi:10.1007/BF01558878.
License Information of Images on page#
| Image Description | Credit | Artist | License Name | File |
|---|---|---|---|---|
| Radiale Elektronendichte in leichten Edelgasatomen mit überlappenden Schalen | https://chem.libretexts.org/Bookshelves/General_Chemistry/Map%3A_A_Molecular_Approach_(Tro)/08%3A_Periodic_Properties_of_the_Elements/8.06%3A_Periodic_Trends_in_the_Size_of_Atoms_and_Effective_Nuclear_Charge | https://chem.libretexts.org/ | Datei:AtomRadialeDichte He, Ne,Ar.jpg | |
| Begriffsklärungs-Icon (Autor: Stephan Baum) | Eigenes Werk ( Originaltext: Own drawing by Stephan Baum ) Original Commons upload as File:Logo Begriffsklärung.png by Baumst on 2005-02-15 | Stephan Baum | Datei:Disambig-dark.svg |







