Isotherme Zustandsänderung
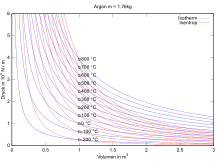
Die isotherme Zustandsänderung ist eine thermodynamische Zustandsänderung, bei der die Temperatur unverändert bleibt:
Bei einer Verdichtung eines Gases muss also die Kompressionswärme abgeführt bzw. bei einer Expansion Wärme zugeführt werden. Dies kann durch ein Wärmebad näherungsweise erreicht werden. Nach dem Gesetz von Boyle-Mariotte und der Zustandsgleichung eines idealen Gases bleibt das Produkt aus Druck und Volumen bei konstanter Temperatur ebenfalls konstant:
- .
Daraus folgt auch, dass sich die Drücke umgekehrt proportional zu den entsprechenden Volumina verhalten:
Für die verrichtete Arbeit gilt bei einer isothermen Kompression oder Expansion von mol eines idealen Gases:
- ,
wobei die Universelle Gaskonstante bezeichnet. Nach dem ersten Hauptsatz der Thermodynamik ( ) folgt mit (und somit ), dass die zugeführte bzw. entzogene Wärme direkt der verrichteten Arbeit entspricht ( ). Daraus folgt , wobei die innere Energie darstellt.
Siehe auch
Weblinks
| adiabatisch | diabatisch · isenthalp · polytrop: isobar | isochor | isotherm | isentrop |