Marfan-Syndrom
| Klassifikation nach ICD-10 | ||
|---|---|---|
| Q87.4 | Marfan-Syndrom | |
| ICD-10 online (WHO-Version 2016) | ||
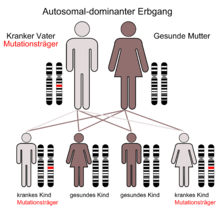
Das Marfan-Syndrom ist eine systemische Besonderheit des Bindegewebes auf der Grundlage einer Genmutation; sie kann autosomal-dominant vererbt werden oder vereinzelt (als Neumutation) auftreten.
Auftrittshäufigkeit
Die Krankheit tritt mit einer Häufigkeit von etwa 1:5.000 bis 1:10.000 auf, wobei sechs bis sieben von zehn Fällen familiär bedingt sind. Der Anteil der Neumutationen beträgt 25 bis 40 %. Da die Definition „Marfan-Syndrom“ derzeit nach Hilfskriterien erfolgt und es mehrere verwechselbare „Parallelkrankheiten“ gibt, sollte besser vom Marfan-Phänotyp gesprochen werden. Dafür insgesamt ist die Häufigkeit etwa 1:6.000. Die Gruppe der Krankheiten des Marfan-Phänotyps wird neuerdings „Fibrillopathien“ genannt.
Erstbeschreibung
Das Syndrom wurde erstmals unter wissenschaftlichen Gesichtspunkten 1896 von dem französischen Kinderarzt Antoine Marfan (1858–1942) beschrieben. Er präsentierte vor der Société Médicale des Hôpitaux de Paris den Fall des fünfjährigen Mädchens Gabrielle, das sehr lange und feine Gliedmaßen aufwies, was er als Dolichostenomelie bezeichnete (griech. „dolicho“ = lang, „stenos“ = schmal, „melos“ = Gliedmaße). Er prägte für die schmalen langen Finger auch den Begriff der Spinnenfingrigkeit (Arachnodaktylie). Sechs Jahre später wurde das Mädchen von den Ärzten Méry und Babonneix untersucht, denen nun auch schon die Röntgen-Diagnostik zur Verfügung stand. Sie beschrieben eine Verkrümmung der Brustwirbelsäule und eine Asymmetrie des Brustkorbs (Thoraxasymmetrie). Ebenfalls 1902 beschrieb Emile Charles Achard ein weiteres Mädchen mit ähnlichen Symptomen und stellte auch eine ausgeprägte Überbeweglichkeit ihrer Gelenke (Hyperlaxizität) fest. Später wurden dem Symptomkomplex noch Veränderungen des Herz-Kreislauf-Systems und der Augen zugeordnet. In den 1930er Jahren erkannte man, dass die Besonderheit nicht geschlechtsgebunden (gonosomal) vererbt wird, sondern dass Veränderungen auf dem Chromosom 15 ursächlich sind (autosomal-dominanter Erbgang). Erstmals wurden diese Veränderungen 1931 von Utrechter Ärzten als Marfan-Syndrom beschrieben, als das es dann in die medizinische Literatur einging.
Das französische Mädchen von Marfans Erstbeschreibung starb allerdings bereits im Jugendalter an Tuberkulose, so dass die Diagnose nie zweifelsfrei bestätigt werden konnte. Hingegen wurde mehrfach angezweifelt, dass Gabrielle an einem Marfan-Syndrom litt, so zuletzt 1972 von Hecht und Beals, die eine kongenitale Arachnodaktylie vermuteten.[1]
Krankheitsursache
Das Gen für das Marfan-Syndrom liegt auf dem langen Arm des Chromosoms 15 (15q21) und ist inzwischen sequenziert. Eine Mutation des Fibrillin-Genes (Fibrillin-1-Gen=FBN1) führt zu einem verkürzten Genprodukt oder einer Missense-Mutation. Mutationen auf dem TGF-β-I- oder TGF-β-II-Gen können zu ähnlichen Symptomen im Rahmen des Loeys-Dietz-Syndroms führen[2].
Merkmale
Feingeweblich manifestiert sich das Marfan-Syndrom in der Feinstruktur des Bindegewebes (der Mikrofibrillen). Das Bindegewebe ist also fehlerhaft aufgebaut, das führt zu einer mehr oder weniger ausgeprägten Instabilität aller Bindegewebe des Körpers.
Folgende Symptome kommen häufig bei Menschen mit Marfan-Syndrom vor, wobei nicht alle Merkmale bei allen Menschen in gleich starker Ausprägung vorliegen:
- Herz- und Gefäßsystem
- Herzklappenfehler (Schlussunfähigkeit der Aorten- oder Mitralklappe – Aneurysma der Aortenwurzel)
- Aortendissektion (Aufspaltung oder Zerreißung der Aortenwand)
- Augen
- Lockerung des Halteapparates der Linsen (Linsenluxation)
- Kurzsichtigkeit
- Glaukom (Grüner Star = hoher Augeninnendruck)
- Katarakt (Grauer Star = Linsentrübung)
- Netzhautablösung: Hierdurch kommt es zu dem Symptom der Lichtblitze (Differentialdiagnose)
- blaue Skleren
- eventuell Iridodonesis (Irisschlottern bei Kopfbewegung)
- Skelettsystem
- senkrechte Überentwicklung des Kopfes (Dolichocephalie/Langschädel)
- Hyperlaxizität (Überstreckbarkeit) der Gelenke
- hoher Gaumen (Gotischer Gaumen)
- Arachnodaktylie (Spinnenfingrigkeit); verschmälerte Finger (Madonnenfinger)
- Trichter- oder Kielbrust
- Hochwuchs
- Verformungen der Wirbelsäule (Skoliose, Hyperkyphose)
- schwach entwickelte Muskulatur (Muskelhypotrophie)
- Plattfüße
- samtartige Haut mit Neigung zu Striae (Dehnungsstreifen)
- Neigung zum Leistenbruch
- Neigung zu atlantoaxialer oder zervikookzipitaler Instabilität, dadurch unter anderem erhöhte Anfälligkeit für das Grisel-Syndrom
- Zu tiefe Hüftpfannen Coxa profunda, erhöhtes Risiko von Schmerzen infolge Impingement sowie von Koxarthrose
- Innere Organe
- Die Bindegewebsschwäche kann auch die Lunge angreifen, wodurch ein so genannter Pneumothorax auftreten kann.
Diagnose und Behandlung
Die Diagnostik und Behandlung sollte stets fachübergreifend (unter anderem durch Kinderkardiologen/Kardiologen, Orthopäden, Augenärzte) erfolgen gemäß der Genter Nosologie (systematische Beschreibung der Krankheiten).
Bislang existiert noch keine ursächlich heilende Therapie.
Einen für die Zukunft denkbaren ursächlichen Therapieansatz zeigten die Ergebnisse einer im April 2006 im Wissenschaftsmagazin Science publizierten Studie, die in einem Mausmodell des Marfan-Syndroms das Zytokin TGF-β mit der typischen Entwicklung von Aortenaneurysmen und -dissektionen in Verbindung bringen konnten. Durch eine Behandlung mit dem als Blutdrucksenker bereits in der Humanmedizin verwandten AT1-Antagonisten Losartan konnten die Mäuse wirksam vor der Ausprägung dieser lebensgefährlichen Veränderungen der Gefäßwand geschützt werden, da Losartan die Wirkung des überaktiven TGF-β antagonisiert. Bereits bestehende Veränderungen am Herzen normalisierten sich zudem weitestgehend, solche in anderen Bereichen des Körpers zumindest teilweise.[3] Eine Studie an über 600 jungen Patienten über die Jahre 2007 bis 2011 zeigt jedoch bezüglich der Vergrößerung der Aortenwurzel keinen signifikanten Unterschied in der Wirkung von Losartan gegenüber der (ohnehin schwachen) Wirkung von Betablockern.[4]
Differentialdiagnose
Bei Vorliegen von Kontrakturen und Auffälligkeiten der Ohrmuschel ist an die Kongenitale Kontrakturale Arachnodaktylie zu denken.
Lebenserwartung
Die größte Bedeutung zur deutlichen Verlängerung der Lebenserwartung fällt in den Bereich der Kinderkardiologie/Kardiologie. Es gibt Hinweise darauf, dass die Geschwindigkeit der Entstehung einer Aortenerweiterung durch die Einnahme von Beta-Blockern vermindert werden kann. Wie weit eine frühe und prophylaktische Einnahme im Kindesalter eine Aortenerweiterung verhindert, ist noch unklar; erste Erfahrungen nach 14 Jahren Beta-Blocker-Therapie bei Kindern (2005), begonnen bei drei- bis vierjährigen betroffenen Kindern, zeigen aber, dass eine Progredienz der Erweiterung der Aortenwurzel in fast allen Fällen nicht eintritt und die Erweiterung unter der Medikation dann nur altersspezifisch erfolgt. Ist die Aortenwurzel bei Erwachsenen auf mehr als 55 mm erweitert, muss eine Operation erfolgen, um eine Aortendissektion oder -ruptur zu verhindern. Dies geschieht evtl. durch einen Aortenwurzelersatz mit künstlicher Herzklappe. Die postoperative Überlebensrate nach zehn Jahren beträgt zwischen 70 und 75 %. Bei Kindern leitet sich die Notwendigkeit einer Operation aus der Abweichung des aktuellen Aortendurchmessers vom altersbezogenen Normalwert ab, der individuell geprüft werden muss. Entscheidend ist, dass bei Kindern und Erwachsenen die Endokarditis-Prophylaxe ganz besonders ernst genommen wird (selbst bei zahnärztlichen Eingriffen, kleinen Wunden, wundgelaufenen Füßen usw.), da eine Besiedlung/Vegetation an den besonders sensiblen Herzklappen und Klappenrändern ein Voranschreiten der Marfan-typischen Gewebeinstabilität auslösen kann.
Bei schweren Verläufen können auch augenärztliche Eingriffe zum Erhalt oder Wiederherstellung der Sehfähigkeit erforderlich werden. Bei Überdehnung und zunehmendem Verlust (Einreißen) der Zonulafasern entsteht das so genannte „Linsenschlottern“. Schlotterlinsen müssen nicht operiert werden, nur das Verschieben der Linsen kann den Augendruck so stark werden lassen, dass die Entfernung der Linse notwendig wird. Es sind inzwischen neue OP-Techniken entwickelt worden, die unter Erhalt des Kapselsackes und Implantation einer Speziallinse bereits bei kleinen Kindern die Sehfähigkeit erhalten kann.
Bei Verläufen mit schweren Wirbelsäulenverbiegungen sind Aufrichtungsoperationen wahrscheinlich. Es sind neue OP-Techniken entwickelt worden, die eine Aufrichtung der Wirbelsäule ohne Vollversteifung ermöglichen.
In den 1970er Jahren ermittelte eine Studie die Lebenserwartung eines Menschen mit Marfan-Syndrom mit 30 bis 40 Jahren. Seit dieser Zeit wurden sowohl die Diagnostik als auch die medikamentöse und chirurgische Behandlung optimiert, so dass die Lebenserwartung sich annähernd der der Normalbevölkerung angeglichen hat. Trotzdem sterben noch immer viele der Betroffenen an einer Dissektion der thorakalen Aorta, weil die Diagnose nicht gestellt wurde und dementsprechend keine Therapie eingeleitet werden konnte.
Literatur
- Mine Arslan-Kirchner, Yskert von Kodolitsch, Jörg Schmidtke: Genetische Diagnostik beim Marfan-Syndrom und verwandten Erkrankungen: Bedeutung des klinischen Managements. In: Dtsch Arztebl. 4. Juli 2008; 105(27), S. 483, doi:10.3238/arztebl.2008.0483, Übersichtsarbeit
- Marfanhilfe (Deutschland) e. V. (Hrsg.): Marfan-Syndrom, Ein Ratgeber für Patienten, Angehörige und Betreuende. Steinkopf, Darmstadt, ISBN 3-7985-1565-4.
- Marfan Stiftung Schweiz (Hrsg.): Herzsache. Gesundheitskompetenz und Empowerment am Beispiel des Marfan-Syndroms. Bern 2008, ISBN 978-3-033-01587-6.
- * R. Witkowski, O. Prokop, E. Ullrich, G. Thiel: Lexikon der Syndrome und Fehlbildungen 7. Auflage. Springer, Berlin 2003, ISBN 3-540-44305-3.
Weblinks
- Marfan Initiative Österreich Informationen für Menschen mit Marfan-Syndrom in Österreich
- Marfan Hilfe (Deutschland) e.V. Verein für Menschen mit Marfan-Syndrom oder anderen mikrofibrillären Erkrankungen
- Marfan Stiftung Schweiz Information, Dokumentation und Beratung für Menschen mit Marfan-Syndrom und verwandten Bindegewebeschwächen
- Genetikzentrum für das Marfan-Syndrom in der Schweiz Genetische Abklärung und Beratung für Menschen mit Marfan-Syndrom und verwandten Aortenkrankheiten
- Marfan Syndrome (engl.) Webseite des Cold Spring Harbor Laboratory mit vielen Animationen und Videos
Quellen
- ↑ Chantal Maron: Marfan: une maladie connue, un pédiatre oublié. In: Le Journal du Médecin (Belgique). 2013, Nr. 2317 vom 10. Mai 2013, S. 17.
- ↑ Loeys-Dietz Syndrome - MeSH - NCBI. Abgerufen am 30. Januar 2014.
- ↑ J. Habashi u. a.: Losartan, an AT1 Antagonist, Prevents Aortic Aneurysm in a Mouse Model of Marfan Syndrome. In: Science. 2006; 312, S. 117–121 (Abstract) (Material und Methoden + sehr beeindruckende Bilder PDF; 462 KB)
- ↑ Sonja Böhm: Eine Hoffnung weniger beim Marfan-Syndrom: Losartan schützt die Aorta nicht besser als ein Betablocker. Medscape, 19. November 2014.
|
|
Dieser Artikel behandelt ein Gesundheitsthema. Er dient nicht der Selbstdiagnose und ersetzt keine Arztdiagnose. Bitte hierzu diesen Hinweis zu Gesundheitsthemen beachten! |