Muskeldystrophie Duchenne
| Klassifikation nach ICD-10 | |
|---|---|
| G71.0 | Muskeldystrophie |
| ICD-10 online (WHO-Version 2019) | |
Die Muskeldystrophie des Typs Duchenne (auch Duchenne-Muskeldystrophie und/oder DMD genannt) ist die häufigste muskuläre Erbkrankheit im Kindesalter. Sie tritt etwa in einer Frequenz von 1:3600 bis 1:6000 auf.[1][2] Aufgrund des X-chromosomal rezessiven Erbganges sind fast nur Jungen betroffen. Auch weibliche Träger dieses Genes können jedoch Symptome zeigen, z. B. im kardialen Bereich, und eine gelegentliche Überwachung auf eine Kardiomyopathie mittels Herzultraschalluntersuchung oder kardialem MRT sowie EKG wird ab einem Alter von 25–30 Jahren für diese Frauen empfohlen.[3][4][5]
Die Duchenne-Muskeldystrophie beginnt im Kleinkindalter mit einer Schwäche der Becken- und Oberschenkelmuskulatur und schreitet rasch voran. Durch optimierte Therapie mit Heimbeatmung und der Anwendung von Cortisonpräparaten bereits im frühen Kindesalter hat sich die Prognose in den letzten Jahren verbessert, und auch die Lebenserwartung ist durch die verbesserte medizinische Versorgung in den letzten Jahren angestiegen.[6] Noch vor wenigen Jahren starben die meisten Patienten im Jugendalter. Heute wird oft das 3. Lebensjahrzehnt erreicht. Die Muskeldystrophie vom Typ Duchenne wurde von Guillaume-Benjamin Duchenne bereits im 19. Jahrhundert in Paris beschrieben.
Ursachen
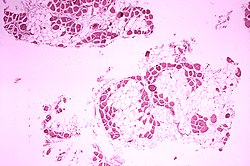
Die Muskeldystrophie Duchenne ist eine genetisch determinierte Synthesestörung des Muskelstrukturproteins Dystrophin. Es wird bei dieser Krankheitsform nicht gebildet. Im Gegensatz dazu wird bei der milder verlaufenden Muskeldystrophie Becker-Kiener Dystrophin in einer zwar verkürzten, jedoch teilweise funktionsfähigen Variante gebildet. Der Dystrophinmangel führt mit der Zeit zum Untergang von Muskelfasern und Ersatz durch Fett- oder Bindegewebe.
Bei der Muskeldystrophie Typ Duchenne ist eine Mutation im Dystrophin-Gen auf dem X-Chromosom (Locus Xp21.2) nachweisbar. Hierbei handelt es sich in 60 bis 70 % um eine Deletion, in ca. 5 % um eine Duplikation und in ca. 35 % um eine Punktmutation. Eine Punktmutation kann auch als Nonsense-Mutation auftreten, hierbei entsteht ein frühzeitiges Stopcodon im Leseraster.[7] Dies tritt bei etwa 10–15 % der Patienten auf.[8] Mehr als 80 % der Mutationen verursachen hierbei eine Verschiebung (Frameshift) des Leserasters und führen damit zu einem kompletten Verlust des Dystrophinproteins. Dabei sind etwa 1/3 der Fälle Neumutationen und nur 2/3 von der nicht manifest erkrankten Mutter (Konduktorin) vererbt.
Symptomatik und Verlauf
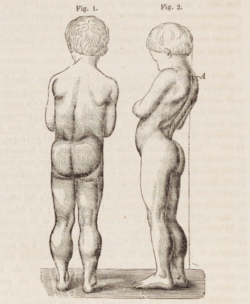
Der Verlauf ist unterschiedlich stark ausgeprägt, aber die frühkindliche Entwicklung ist zunächst in der Regel normal. Je nach Stärke der Erkrankung kann ab dem 3. bis 5. Lebensjahr eine leichte Muskelschwäche der Beine auffallen, die zu häufigem Stolpern und Fallen führt. Im weiteren Verlauf kann das Treppensteigen nur noch mit Zuhilfenahme eines Geländers möglich sein. Die Muskelschwäche der Becken- und Oberschenkelmuskulatur kann zu einem Watschelgang (Trendelenburgzeichen) führen sowie das Aufrichten aus dem Sitzen oder Liegen erschweren. Die Kinder stützen sich auf ihre Oberschenkel auf beim Aufrichten (Gowers-Manöver) oder nutzen Wände und Möbel zum Abstützen. Bei schweren Formen sind ab dem 5. bis 7. Lebensjahr das Treppensteigen und Aufstehen aus dem Sitzen oder Liegen nur noch mit Hilfe anderer möglich, da die Erkrankung auch auf die Muskulatur der Schulter und Arme übergreift. Zwischen dem 7. und 12. Lebensjahr ist ein Anheben der Arme in die Waagerechte kaum mehr möglich. Viele Kinder sind in diesem Alter bereits auf den Rollstuhl angewiesen, können sich aber noch eingeschränkt selbständig versorgen. Oftmals besteht bei schweren Verläufen ab dem 18. Lebensjahr eine vollständige Pflegebedürftigkeit.
Infolge des Muskelschwundes kommt es zu schmerzhaften Fehlstellungen von Gelenken und Knochenverformungen. Charakteristisch für den Typ Duchenne sind die sogenannten „Gnomen-“ oder „Kugelwaden“. Sie entstehen durch Fetteinlagerungen in der bindegewebig umgebauten Unterschenkel-Muskulatur (Pseudohypertrophie). Bei Abbau der Schultergürtelmuskulatur kommt es zu hervorstehenden Schulterblättern („Scapulae alatae“), auch Engelsflügel genannt. Durch Schwäche der Atemmuskulatur wird das Abhusten, bei Infekten der Luftwege, deutlich erschwert und dadurch kann die Lebenserwartung erheblich eingeschränkt werden. Der Herzmuskel ist zwar meist vom Krankheitsprozess betroffen, doch führen erhöhte Herzfrequenz und sonstige Veränderungen des Rhythmus oder auch Beeinträchtigung der Herzkraft selten zu subjektiven Beschwerden. Die Lebenserwartung der Patienten beträgt je nach Verlauf etwa 40 Jahre, jedoch versterben einzelne Patienten auch schon vor Beginn der Pubertät.
In 50–95 % der Fälle bildet sich auch eine seitliche Verkrümmung der Wirbelsäule (Skoliose), die etwa dann einsetzt, wenn die Gehfähigkeit verloren geht, meist zwischen 10 und 14 Jahren. Bei etwa 85 % der betroffenen Kinder kommt es anfangs zu einer Progression der Skoliose mit mittlerer Zunahme des Cobb-Winkels, der das Ausmaß der Fehlstellung beschreibt, um monatlich 2,1°. Hierdurch wird auch die Lungenfunktion beeinträchtigt und die forcierte Vitalkapazität (FVC) sinkt im Sinne einer restriktiven Lungenfunktionsstörung um etwa 4 % pro 10° Zunahme der Skoliose. Es besteht die Möglichkeit, durch eine langstreckige Versteifung der Wirbelsäule (Spondylodese), die Progression und die Verminderung des Lungenvolumens aufzuhalten. Der Eingriff ist aber mit Risiken verbunden und sein Stellenwert ist nicht klar. Eine schottische retrospektive Studie untersuchte die Komplikationsrate bei 26 posterioren Spondylodese-Operationen. Im Mittel waren die Jungen 14,2 Jahre alt, die Operation dauerte mittlere 260 Minuten, der mittlere postoperative Aufenthalt auf der Intensivstation betrug fünf Tage, der Krankenhausaufenthalt im Mittel fünfzehn Tage. Komplikationen zeigten sich deutlich häufiger als bei vergleichbaren Operationen bei anderen Grunderkrankungen und bestanden bei 10 Kindern (39 %), davon vier akuten Leberschäden (Hepatotoxizität, mit vollständiger Besserung bei allen Kindern im weiteren Verlauf) und fünf tiefen Wundinfektionen.[9]
Diagnostik
Der Verdacht auf Muskeldystrophie ergibt sich, wenn im Kindesalter eine ungewöhnliche, symmetrisch ausgebildete Schwäche der Muskulatur beobachtet wird. Bei der Anamnese interessieren besonders der Beginn der Funktionsstörungen, der Verlauf und das Auftreten ähnlicher Störungen in der Familie, besonders bei männlichen Verwandten der Mutter. Im Rahmen der körperlichen Untersuchung wird nach allgemeinen Auffälligkeiten geschaut, wie Haltung, Beweglichkeit und Atmung. In der neurologischen Untersuchung wird die Funktion der Nerven und Muskeln überprüft.
Laborwerte geben wichtige Hinweise – die Konzentration der Transaminasen ist oft erhöht, vor allem aber ist die Konzentration der Creatin-Kinase, einem Muskelenzym, stark erhöht, oft auf Werte oberhalb des 10-100fachen des Normbereiches. Ein erhöhter Creatin-Kinase Wert ersetzt jedoch nicht eine weitere Diagnostik, da es auch andere Ursachen geben kann.
Zu den üblichen Zusatzuntersuchungen gehören die Elektroneurographie, bei der die Nervenleitgeschwindigkeit bestimmt wird, und die Elektromyographie, die unterscheiden hilft, ob eine primäre Muskelerkrankung oder eine Erkrankung der motorischen Nerven die Ursache der Schwäche ist. Als bildgebende Verfahren werden MRT und Ultraschall eingesetzt. Hier können ohne Belastung des Patienten strukturelle Veränderungen der Muskeln beurteilt werden. Die Muskelbiopsie erlaubt die Untersuchung des Muskels unter dem Licht- oder Elektronenmikroskop. Die Stoffwechselvorgänge im Muskel können damit genau untersucht werden. Die Gendiagnostik bestätigt die Diagnose und macht eine genaue Zuordnung nach Typus möglich. Diese genetische Diagnostik ist unter anderem wichtig, weil sie Informationen ermöglicht, welche Therapie möglich ist. Nicht alle Therapien sind für alle Patienten mit Duchenne geeignet.
Bedeutung der Atemfunktion
Viele der Todesfälle bei DMD-Patienten sind durch eine Abnahme der Atemfunktion bedingt.[10][11] Die Früherkennung des Atemfunktionsverlusts bei DMD ist daher sehr entscheidend. Im Frühstadium verläuft die abnehmende Atemfunktion asymptomatisch. Bei Funktionseinschränkungen der Atemfunktion (FVC und PEF) fallen die Messwerte meistens pro Jahr um rund 5 % ab. DMD-Patienten mit Einschränkungen der Atemfunktion tragen ein erhöhtes Risiko für – mitunter schwere und lebensbedrohliche – Atemwegsinfektionen. Zur Vermeidung von Atemwegsinfekten durch angesammelten Schleim (nicht nur im Rahmen von Erkältungen) können Systeme eingesetzt werden, die zu einer Hustenunterstützung führen. Dabei wird per automatischem Luftstrom Luft in die Lunge geleitet und rasch wieder herausgesaugt, was ein Abhusten sehr effizient erleichtert. Aktuelle therapeutische Optionen können die fortschreitende Abnahme der Atemfunktion bei DMD nicht ausreichend beeinflussen. Regelmäßiges Monitoring der Atemfunktion erhöht die Chancen, die Progression durch frühe Interventionen zu verlangsamen. Der zunehmende Verlust an Muskelkraft reduziert die Atemfunktion irreversibel und verantwortet dadurch viele Todesfälle bei DMD.
Lungenfunktionsmessungen werden in den meisten Zentren bei den Patienten erstmals im Alter von ungefähr sechs Jahren durchgeführt und dann jährlich wiederholt. Die Werte sind in diesem Alter meist noch nicht auffällig. Um das Risiko der Entwicklung einer Atempumpenschwäche zu verfolgen und rechtzeitig – und nicht erst im Fall einer respiratorischen Dekompensation – eine Atempumpenschwäche zu diagnostizieren, empfiehlt die Deutsche Gesellschaft für Pneumologie in ihrer Leitlinie ein Lungenfunktionsscreening in regelmäßigen Abständen (alle 3-12 Monate je nach klinischem Verlauf und vorliegender neuromuskulärer Erkrankung).[12] Ab einem Alter von zwölf Jahren (bzw. dem Verlust der Gehfähigkeit) wird die FVC-Messung zweimal jährlich empfohlen – allerdings erhalten nur ca. 50 % der Patienten diesen Alters dieses Lungenfunktions-Monitoring.[13] Es ist wichtig, auch bei Patienten im Rollstuhl die Überprüfung der Lungenfunktionswerte regelmäßig durchzuführen, da sie wichtige Entscheidungen unterstützen, die sich sehr positiv auf die Erkrankung auswirken.[4][14][15]
Je früher interveniert und damit versucht wird, die Abnahme der Atemfunktion aufzuhalten, desto höher ist die Chance, dass die bisher noch unvermeidliche Progression langsamer voranschreitet. Dies könnte – wenn auch durch klinische Daten noch nicht belegt – eventuell auch die Verlängerung einer höheren Lebensqualität für die Patienten bedeuten, denn im Rollstuhl sitzende Patienten bezeichnen die Abnahme der Atemfunktion als ihre größte Sorge.
Therapie
Eine Heilung der Erkrankung ist bisher nicht möglich. Seit 2024 ist in den USA der Wirkstoff Givinostat (Duvyzat, Hersteller: Italfarmaco) zugelassen. Der Histon-Deacetylase(HDAC)-Hemmer kann den Krankheitsverlauf durch Reduktion von Entzündungsvorgängen verzögern.[16] In der EU hat der Wirkstoff den Status eines Orphan-Arzneimittels.[17]
Die Therapie erfolgt weiterhin symptomatisch, um die Folgen der Muskeldystrophie abzumildern, ein Voranschreiten aufzuhalten und Komplikationen zu behandeln. Eine effektive Behandlung erfolgt multidisziplinär und bedarf einer Zusammenarbeit von Arzt, Physiotherapie, Ergotherapie, Orthopädietechnik und Pflege, oft auch mit psychologischer Unterstützung für die Betroffenen und ihre Angehörigen.
Ziel aller physiotherapeutischen Maßnahmen ist es, die Folgen der Muskelschwäche so gering wie möglich zu halten bzw. in einem bestimmten Ausmaß zu korrigieren. Sport sollte durchaus erfolgen, jedoch in einer Weise, die bei Gesunden niemals zu Muskelkater führen würde. Gewissermaßen ist die Fähigkeit von Duchenne Patienten, sich nach einem Muskelkater zu erholen, enorm eingeschränkt. Mäßiges Training ist jedoch sinnvoll und verzögert z. B. die Skoliose.[4] Durch ökonomisches Training mit leichter bis mäßiger Belastung wie Gehen, Schwimmen und Fahren auf dem Ergometer ist eine Verbesserung der Ausdauer und damit eine Minderung der Schwäche zu erreichen. Kortisongaben und operative Lösung von Kontrakturen verlängern die Gehfähigkeit, Kreatin kann eine diskrete Verbesserung des Muskelenergiestoffwechsels bewirken (regelmäßige Therapiepausen nötig). Eine sich entwickelnde Skoliose (Verkrümmung der Wirbelsäule) kann durch die Implantation von Metallstäben (Harrington-Stab) operativ begradigt werden; hierdurch wird vor allem die Atemfunktion verbessert. Seit 1989 werden mitwachsende Teleskopstäbe eingesetzt.
Als Hilfsmittel werden Orthesen, Rollstuhl, Duschstuhl, Badewannenlifter, Toilettensitzerhöhungen und Rollstuhlrampen eingesetzt.
Atmungsunterstützung
Da durch die zunehmende Schwäche der Atemmuskulatur die Eigenatmung immer weiter abnimmt, kommt es zunächst zu nächtlichen Atemproblemen. Dies äußert sich zum Beispiel in Tagesschläfrigkeit, mangelndem morgendlichen Appetit, Konzentrationsschwierigkeiten und Antriebslosigkeit.[14] Es kann zwischen dem durchschnittlichen Alter von 18 und 20 Jahren eine maschinelle Beatmung notwendig werden.[18] Dies erfolgt überwiegend nicht-invasiv mit einem CPAP-Gerät über eine Nasen- oder Nasen-Mund-Beatmungsmaske. Die Durchführung einer Tracheotomie ist anfangs meist nicht notwendig und wird normalerweise erst dann durchgeführt, wenn der Patient auch tagsüber auf die Beatmung angewiesen ist. Von einer generellen Tracheotomierung ist man inzwischen weitgehend abgerückt. Besonders zu beachten ist auch, ob sich eine Abhustschwäche entwickelt, die konsequent durch Hustenunterstützungssysteme behandelt werden sollte, um das Infektionsrisiko zu senken. Durch physiotherapeutische Techniken (Atemtraining und/oder apparative Maßnahmen) ist im Bereich der Atmung derzeit viel Unterstützung möglich.[15] Sobald die Krankheit auf die Atemmuskulatur übergreift, müssen regelmäßige Lungenfunktionstests erfolgen. In den letzten Jahren wurden gute Fortschritte in der Möglichkeit der Heimbeatmung gemacht. Bei der Erstellung eines Trainingsprogramms muss die Herzbelastbarkeit überprüft werden.
Glukokortikoide
Glukokortikoide wirken sich positiv aus und führen zu einer Verzögerung des Krankheitsverlaufes und des Verlusts der Gehfähigkeit von etwa 3 Jahren.[19] Mit Vamorolon (Amgree, Hersteller: Santhera Pharmaceuticals) ist seit 2023 in der EU und den USA ein Arzneistoff aus der Gruppe der Corticosteroide für die Behandlung der Muskeldystrophie Duchenne zugelassen, der eine mit Prednison vergleichbare Wirksamkeit, jedoch ein günstigeres Nebenwirkungsprofil hat.[20] Deflazacort (Emflaza) ist seit 2017 in den USA für die Indikation Muskeldystrophie Duchenne zugelassen.[21]
Ataluren
Ein weiterer Ansatz beruht darauf, das defekte Gen trotz der Mutation vollständig auszulesen. Dies soll z. B. mit Hilfe von Ataluren bei etwa 10-15 % der Patienten möglich sein.[8] Daher ist eine genaue Mutationsbestimmung sehr wichtig für die Erwägung einer Therapie mit Ataluren.
Der Wirkstoff wird für die Behandlung der Duchenne-Muskeldystrophie infolge einer Nonsense-Mutation im Dystrophin-Gen bei gehfähigen Patienten im Alter ab 2 Jahren angewendet.[22] Die Interaktion von Ataluren und dem Ribosom bewirkt, dass anstelle des Stopp-Codons eine Aminosäure eingefügt wird. Dies ermöglicht es dem Ribosom, den Translationsprozess (die Synthese von Dystrophin-mRNA) weiter fortzusetzen. Auf diese Weise kann die genetische Information trotz Nonsense-Mutation weiter abgelesen und das Zielprotein in geringen Mengen erzeugt werden.[23][24] Studien zufolge bleibt die Gehfähigkeit bei Patienten, die mit Ataluren behandelt werden, um bis zu fünf Jahre länger (im Schnitt bis zum Alter von 16,5 Lebensjahre) erhalten als bei unbehandelten Duchenne-Patienten im Rahmen des natürlichen Krankheitsverlaufs.[25][26][27] Wenn die therapeutischen Maßnahmen zu einem Zeitpunkt beginnen, zu dem noch eine ausreichende regenerative Kapazität der Muskulatur gewährleistet ist, kann die Muskelfunktion und die Gehfähigkeit so lange wie möglich erhalten und die Progression der Erkrankung verlangsamt werden.[28][29] Je länger es gelingt, die Gehfähigkeit der betroffenen Jungen zu erhalten, umso weiter lässt sich auch der Abfall der pulmonalen Kapazität hinauszögern. Denn dieser erfordert im fortgeschrittenen Erkrankungsstadium eine Beatmung der Patienten.[30]
Klinische Entwicklung
Verschiedene Firmen entwickeln neuartige Substanzen zur Behandlung der DMD, u. a.:
- Das Unternehmen Sarepta Therapeutics untersucht Eteplirsen / EXONDYS 51 (Phase IV): es ist in den USA bereits zur Behandlung der DMD zugelassen. Hierbei handelt es sich um ein Medikament für das sogenannte Exon-Skipping, bei dem erreicht wird, dass es zu einer milderen Verlaufsform von Duchenne-Muskeldystrophie kommt, dies bei nach genetischer Testung geeigneten Patienten. In Europa steht die Zulassung noch aus.[31]
- Das bereits in der Leberschen Optikusatrophie (LHON) zugelassene und auf die Mitochondrien wirkende Medikament Idebenon / Raxone wurde von der Herstellerfirma Santhera in mehreren Studienprogrammen zu DMD untersucht.[32] Eine Zulassung bei der europäischen Arzneimittelbehörde (EMA) wurde im Mai 2019 beantragt.[33] Im Rahmen des Studienprogramms wurde für Patienten ab 10 Jahren eine verringerte Abnahme der Atemfunktion über einen längeren Zeitraum belegt.[34] Die Firma Santhera führte eine klinische Studie durch, bei der die Wirksamkeit von Idebenon zusätzlich zu einer weiter durchgeführten Standardbehandlung mit Glucocorticoiden verglichen wurde mit der Standardbehandlung mit Glucocorticoiden alleine. Im Rahmen einer vorzeitig durchgeführten Interimsanalyse zeigte sich, dass es voraussichtlich mit der Anzahl der Patienten und im angestrebten Behandlungszeitraum nicht zu einem signifikanten Vorteil beim primären Endpunkt (Forcierte Vitalkapazität in % des Soll, FVC%p) kommen würde. Daraufhin wurde das gesamte Zulassungsprogramm von Idebenon bei Duchenne gestoppt.[35] Dies betraf auch den zu dem Zeitpunkt bereits laufenden Zulassungsantrag zu Idebenon in Monotherapie.[35]
- Bristol-Myers Squibb kooperiert mit Biogen und Roche in der Entwicklung von BMS-986089 zur Behandlung von DMD.[36]
- Die Firma Reveragen hat ein Medikament in der klinischen Testung (Phase III), das als ein neuartiges Glukokortikoid wirkt bei einem verbesserten Nebenwirkungsprofil.[37]
- Catabasis Pharmaceuticals untersuchte die Wirksamkeit des eigens entwickelten Wirkstoffs Edasalonexent im Rahmen einer klinischen Studie (Phase III).[38] Die erste Beurteilung dieser Studie zeigte keinen Vorteil des Medikamentes beim primären Endpunkt, wodurch das Entwicklungsprogramm gestoppt wurde, auch mit Auswirkungen auf die Studie GalaxyDMD (offene Verlängerungsstudie von PolarisDMD).[39]
Einzelnachweise
- ↑ Flotats-Bastardas M, Ebrahimi-Fakhari D, Bernert G, Ziegler A, Schlachter K, Poryo M, Hahn A, Meyer S.: Nichtgehfähige Patienten mit Duchenne-Muskeldystrophie. In: Der Nervenarzt. 90. Jahrgang, Nr. 8, August 2019, S. 817–823, doi:10.1007/s00115-019-0754-y (springer.com).
- ↑ 23. Mah JK, Korngut L, Dykeman J et al: A systematic review and meta-analysis on the epidemiology of Duchenne and Becker muscular dystrophy. In: NeuromusculDisord. 24. Jahrgang, Nr. 6, Juni 2014, S. 482–491, doi:10.1016/j.nmd.2014.03.008 (nmd-journal.com).
- ↑ Birnkrant DJ, Bushby K, Bann CM et al: Diagnosis and management of Duchenne muscular dystrophy, part 1: diagnosis, and neuromuscular, rehabilitation, endocrine, and gastrointestinal and nutritional management. In: The Lancet Neurology. 17. Jahrgang, Nr. 3, März 2018, S. 251–267, doi:10.1016/S1474-4422(18)30024-3 (thelancet.com).
- 1 2 3 Birnkrant DJ, Bushby K, Bann CM et al: Diagnosis and management of Duchenne muscular dystrophy, part 2: respiratory, cardiac, bone health, and orthopaedic management. In: The Lancet Neurology. 17. Jahrgang, Nr. 4, April 2018, S. 347–361, doi:10.1016/S1474-4422(18)30025-5 (thelancet.com).
- ↑ Birnkrant DJ, Bushby K, Bann CM et al: Diagnosis and management of Duchenne muscular dystrophy, part 3: primary care, emergency management, psychosocial care, and transitions of care across the lifespan. In: The Lancet Neurology. 17. Jahrgang, Nr. 5, März 2018, S. 445–455, doi:10.1016/S1474-4422(18)30026-7 (thelancet.com).
- ↑ Deutsche Gesellschaft für Muskelkranke e. V. DGM: Erklärvideo Muskeldystrophien Duchenne und Becker. 18. April 2018, abgerufen am 19. November 2018.
- ↑ Rosenberg AS et al. Sci Transl Med. 2015; 7:299rv4.
- 1 2 Muntoni F, Desguerre I, Guglieri M, Osorio AN, Kirschner J, Tulinius M, Buccella F, Elfring G, Werner C, Schilling T, Trifillis P, Zhang O, Delage A, Santos CL, Mercuri E.: Ataluren use in patients with nonsense mutation Duchenne muscular dystrophy: patient demographics and characteristics from the STRIDE Registry. In: J Comp Eff Res. 8. Jahrgang, Nr. 14, August 2019, S. 445–455, doi:10.2217/cer-2019-0086 (futuremedicine.com).
- ↑ A. D. Duckworth, M. J. Mitchell, A. I. Tsirikos: Incidence and risk factors for post-operative complications after scolioses surgery in patients with Duchenne muscular dystrophy. The Bone & Joint Journal 2014, Band 96-B, Ausgabe 6 vom Juli 2014, Seiten 943–949; doi:10.1302/0301-620X.96B7.33423
- ↑ Henricson EK et al.: The cooperative international neuromuscular research group Duchenne natural history study; Muscle Nerve 2013; Band 48, Seiten 55–67; doi:10.1002/mus.23808
- ↑ Mayer OH et al.: Characterization of pulmonary function in Duchenne Muscular Dystrophy; Pediatr Pulmonol 2015; Band 50, Seiten 487–94; doi:10.1002/ppul.23172
- ↑ S2k-Leitlinie: Nichtinvasive und invasive Beatmung als Therapie der chronischen respiratorischen Insuffizienz – Revision 2017, abgerufen am 2. Dezember 2019.
- ↑ Andrews JG et al.: Respiratory Care Received by Individuals With Duchenne Muscular Dystrophy From 2000 to 2011, Respir Care 2016; Band 61, Seiten 1349–59.
- 1 2 Daniel W. Sheehan, David J. Birnkrant, Joshua O. Benditt, Michelle Eagle, Jonathan D. Finder, John Kissel, Richard M. Kravitz, Hemant Sawnani, Richard Shell, Michael D. Sussman and Lisa F. Wolfe: Respiratory Management of the Patient With Duchenne Muscular Dystrophy. In: Pediatrics. 142. Jahrgang, Nr. 2, Oktober 2018, S. 62–71, doi:10.1542/peds.2018-0333H (aappublications.org).
- 1 2 www.aktionbenniundco.de, Website aktion Benni & Co e. V., abgerufen am 2. Dezember 2019.
- ↑ Sven Siebenand: US-Zulassung für Givinostat. In: pharmazeutische-zeitung.de. 10. April 2024, abgerufen am 26. Mai 2024.
- ↑ Eintrag EU/3/12/1009 im Unionsregister für Orphanarzneimittel. In: ec.europa.eu. 4. Juli 2012, abgerufen am 26. Mai 2024 (englisch).
- ↑ Anita K. Simonds: Recent advances in respiratory care for neuromuscular disease. In: Chest. Band 130, Dezember 2006, S. 1881, Abschnitt DMD, doi:10.1378/chest.130.6.1879.
- ↑ Craig M. McDonald et al.: Long-term effects of glucocorticoids on function, quality of life, and survival in patients with Duchenne muscular dystrophy: a prospective cohort study. In: Lancet. Band 391, Nr. 10119, 2018, S. 451–461, doi:10.1016/s0140-6736(17)32160-8, PMID 29174484.
- ↑ Michela Guglieri et al.: Efficacy and Safety of Vamorolone vs Placebo and Prednisone Among Boys With Duchenne Muscular Dystrophy. In: JAMA neurology. Band 79, Nr. 10, 2022, S. 1005–1005, doi:10.1001/jamaneurol.2022.2480, PMID 36036925.
- ↑ Office of the Commissioner: FDA approves drug to treat Duchenne muscular dystrophy. In: fda.gov. 9. Februar 2017, abgerufen am 26. Mai 2024 (englisch).
- ↑ Europäische Arzneimittel-Agentur: Translarna (ataluren). In: Europäische Arzneimittel-Agentur. 17. September 2018, abgerufen am 24. Oktober 2019 (englisch).
- ↑ Bushby K et al. Muscle Nerve 2014; 50: 477–487.
- ↑ Haas M et al. Neuromuscul Disord. 2015; 25:5–13.
- ↑ Delage et al. Effect of ataluren on age at loss of ambulation in nonsense mutation Duchenne muscular dystrophy: observational data from the STRIDE Registry. Poster presented at The 23RD International Annual Congress of the World Muscle Society Congress, 2.–6. Oktober 2018, Mendoza, Argentinien.
- ↑ Bello L et al. Neurology 2016; 87(4): 401-09.
- ↑ Delage et al. Long-term efficacy of ataluren for the treatment of nonsense mutation Duchenne muscular dystrophy: observational data from the STRIDE Registry. Poster presented at The 23RD International Annual Congress of the World Muscle Society Congress, 2.–6. Oktober 2018, Mendoza, Argentinien.
- ↑ Merlini L und Sabatelli P. BMC Neurol. 2015; 15:153.
- ↑ Rosenberg AS et al. Sci Transl Med. 2015; 7:299rv4.
- ↑ Humbertclaude V et al. Eur J Paediatr Neurol. 2012; 16:149-60.
- ↑ FDA grants accelerated approval to first drug for Duchenne muscular dystrophy, PM FDA vom 19. September 2016, abgerufen am 29. Juni 2018.
- ↑ Idebenon bei DMD ( des vom 27. Juni 2018 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis., Website des Herstellers, abgerufen am 29. Juni 2018.
- ↑ Santhera reicht Zulassungsantrag bei der Europäischen Arzneimittelbehörde für Puldysa® (Idebenon) bei Duchenne-Muskeldystrophie ein, PM Santhera vom 27. Mai 2019, abgerufen am 3. Dezember 2019.
- ↑ Servais L, Straathof C, Schara U, Klein A, Leinonen M, Hasham S, Meier T, de Waele L, Gordish-Dressman H, McDonald C, Mayer O, Voit T, Mercuri E, Buyse G for the SYROS and CINRG DNHS Investigators: Long-term data with idebenone on respiratory function outcomes in patients with Duchenne muscular dystrophy. In: Neuromusc Disorder. 29. Jahrgang, Nr. 10, Oktober 2019, doi:10.1016/j.nmd.2019.10.008 (nmd-journal.com).
- 1 2 Santhera to Discontinue Phase 3 SIDEROS Study and Development of Puldysa® in Duchenne Muscular Dystrophy (DMD) and Focus on Vamorolone, PM Santhera vom 6. Oktober 2020, abgerufen am 5. November 2020.
- ↑ Bristol-Myers Squibb Enters into Separate Agreements with Biogen and Roche to License Anti-eTau and Anti-Myostatin Compounds, Respectively, PM BMS vom 13. April 2017, abgerufen am 29. Juni 2018.
- ↑ Eric P. Hoffman, Benjamin D. Schwartz, Laurel J. Mengle-Gaw, Edward C. Smith, Diana Castro, Jean K. Mah, Craig M. McDonald, Nancy L. Kuntz, Richard S. Finkel, Michela Guglieri, Katharine Bushby, Mar Tulinius, Yoram Nevo, Monique M. Ryan, Richard Webster, Andrea L. Smith, Lauren P. Morgenroth, Adrienne Arrieta, Maya Shimony, Catherine Siener, Mark Jaros, Phil Shale, John M. McCall, Kanneboyina Nagaraju, John van den Anker, Laurie S. Conklin, Avital Cnaan, Heather Gordish-Dressman, Jesse M. Damsker, Paula R. Clemens, the Cooperative International Neuromuscular Research Group: Vamorolone trial in Duchenne muscular dystrophy shows dose-related improvement of muscle function. In: Neurology. 93. Jahrgang, Nr. 13, September 2019, S. e1312-e1323, doi:10.1212/WNL.0000000000008168 (neurology.org).
- ↑ PolarisDMD CLINICAL TRIAL, Website Catabasis, abgerufen am 5. November 2020.
- ↑ Catabasis Pharmaceuticals Announces Top-Line Results For The Phase 3 PolarisDMD Trial Of Edasalonexent In Duchenne Muscular Dystrophy, PM Catabasis vom 26. Oktober 2020, abgerufen am 5. November 2020.
License Information of Images on page#
| Image Description | Credit | Artist | License Name | File |
|---|---|---|---|---|
| Drawing of 7-year-old boy with Duchenne muscular dystrophy. There is excessive development of the lower limbs (pseudohypertrophy), and thinness of the arms. In the figure on the right, lumbar hyperlordosis is visible. | 1868. "De la paralysie musculaire pseudo-hypertrophique, ou paralysie myo-sclérosique". Arch. Gen. Med. (in French). Bibliothèque nationale de France. 11: 5–25, 179–209, 305–321, 421–443, 552–588. Retrieved 18 May 2020. https://gallica.bnf.fr/ark:/12148/bpt6k851346p.image | Duchenne, Guillaume-Benjamin | Datei:Drawing of boy with Duchenne muscular dystrophy.png | |
| Histopathologisches Bild eines Querschnitts aus dem Wadenmuskel (Muskulus gastrocnemius) eines Patienten, der an Muskeldystrophie Typ Duchenne verstarb. Das Bild verdeutlicht, in welchem Ausmaß die (rot gefärbten) Muskelfasern durch Fettzellen (optisch leer = weiß) ersetzt wurden. | http://phil.cdc.gov/phil/home.asp ID#: 70 US Department of Health and Human Services Dieses Medium stammt aus der Public Health Image Library (PHIL), mit der Identifikationsnummer #70 der Centers for Disease Control and Prevention . Hinweis: Nicht alle PHIL-Bilder sind gemeinfrei; überprüfe unbedingt den Urheberrechtsstatus und die Nennung der Autoren und Inhaltsanbieter. العربية Deutsch English македонски slovenščina +/− | Dr. Edwin P. Ewing, Jr. | Datei:Duchenne-muscular-dystrophy.jpg | |
| The Rod of Asclepius overlaid with a caution symbol | Star of life caution.svg with Nuvola apps important.svg | Gigillo83 | Datei:P medicine caution.svg | |
| Piktogramm zum Kennzeichnen von Informationen bei einer Wahl/Abstimmung. | Own illustration, 2007 | Arne Nordmann ( norro ) | Datei:Pictogram voting info.svg |

