P-v-Diagramm
Das p-v-Diagramm ist eine spezielle Form eines Zustandsraums eines Gases (bzw. Fluids), bei der der Druck p eines Systems gegen das spezifische Volumen v aufgetragen wird. Ein bestimmtes Gas ist somit immer durch einen Punkt auf dem p-v-Diagramm beschrieben. Verwendet man anstatt des spezifischen Volumens v das Volumen V, so spricht man auch von einem p-V-Diagramm; in diesem Fall ist der Bezug auf eine gleich bleibende Stoffmenge bzw. Masse nicht mehr gegeben und muss gegebenenfalls als zusätzliche Forderung erhoben werden.
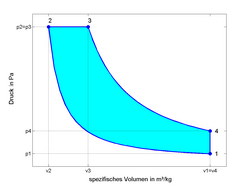
Das p-v-Diagramm wird häufig dazu verwendet, um Prozessabläufe – mit oder ohne Phasenumwandlung – zu veranschaulichen, wie rechts beispielhaft am Diesel-Prozess dargestellt. Druck und Volumen des Fluides können sich unter unterschiedlichen Prozessanforderungen ändern, beispielsweise isobar (konstanter Druck) oder isochor (konstantes Volumen). Das Fluid läuft dann die entsprechende Strecke im p-v-Diagramm entlang. Werden unterschiedliche Zustandsänderungen nacheinander durchgeführt und dieser Vorgang kontinuierlich wiederholt, spricht man von einem Kreisprozess.
Gemäß der Gibbsschen Phasenregel hat ein reines Fluid beziehungsweise ein Fluidgemisch mit konstanter Zusammensetzung genau zwei Freiheitsgrade. Daraus folgt, dass in der Funktion der Druck p eindeutig durch das spezifische Volumen v und die Temperatur T beschrieben wird.
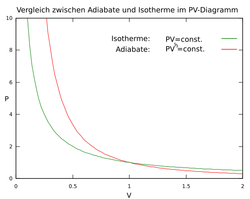
Trägt man diesen Zusammenhang in ein dreidimensionales Diagramm ein, so entsteht ein p-V-T-Diagramm. Durch Projektion dieser Oberfläche in die p-V-Ebene erhält man ein p-V-Diagramm. Hierbei ist der Druck p die Ordinate, das spezifische Volumen v die Abszisse und die Temperatur T wird je nach Anwendung für den Graphen konstant gewählt (Isotherme) oder vernachlässigt .
In dieses Diagramm werden häufig auch die Grenzen der Aggregatzustände „fest“, „flüssig“ und „gasförmig“ beziehungsweise die einzelnen Phasen des Fluids eingetragen.
Siehe auch
Literatur
- Hans Joachim Eichler, Heinz-Detlef Kronfeldt, Jürgen Sahm: Das Neue Physikalische Grundpraktikum. Springer Verlag, Berlin/Heidelberg 2001, ISBN 3-662-21754-6.
- Jürgen Zeitler, Günter Simon: Physik für Techniker. 7., aktualisierte Auflage. Fachbuchverlag Leipzig im Carl Hanser Verlag, München 2013, ISBN 978-3-446-43377-9.
Weblinks
- Zustandsänderungen Vorlesungsskript (abgerufen am 21. Januar 2016)
- Zustandsgebiet im p - v T -Diagramm (abgerufen am 21. Januar 2016)
License Information of Images on page#
| Image Description | Credit | Artist | License Name | File |
|---|---|---|---|---|
| Vergleich von Adiabate und Isotherme im PV-Diagramm für ein ideales Gas: Adiabate: P ⋅ V 5 3 = c o n s t . \displaystyle P\cdot V^5 \over 3=const. d S = 0 \displaystyle dS=0 und C V = c o n s t . \displaystyle C_V=const. Isotherme: P ⋅ V = n ⋅ R ⋅ T = c o n s t . \displaystyle P\cdot V=n\cdot R\cdot T=const. | Eigenes Werk ( Originaltext: Selbst gezeichnet ) | Benutzer:Sgbeer | Datei:Adiabate-Isotherme.png | |
| Pv-Diagramm idealer Dieselprozess | Übertragen aus de.wikipedia nach Commons durch Leyo mithilfe des CommonsHelper . Eigenes Werk | Poelsermampfer in der Wikipedia auf Deutsch | Datei:PvDiagramm-Diesel 0110.png |

